FDA 警告書が頻繁に指摘するスプレッドシートの脆弱性
ラボは常に生産性を重視することで投資利益率を最大化し、FDA 監査によるコスト面での影響を回避すると同時に、コンプライアンス戦略に関する基本的な問題には容易に対処できるようにしておく必要があります。対策のために選ぶツールは、コンプライアンスプログラムの効果とコンプライアンスの達成度に直接、影響を及ぼす可能性があります。
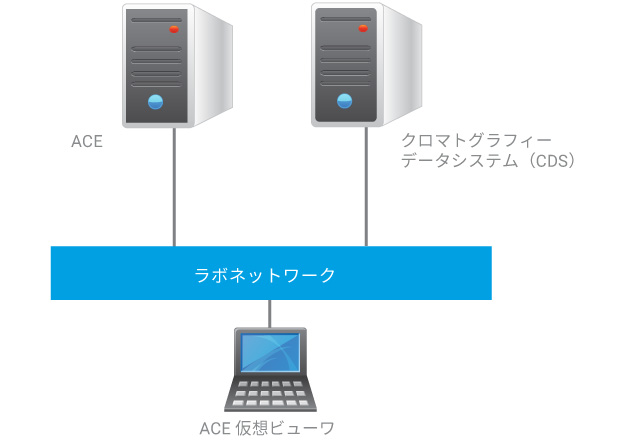
特に、製薬業界における規制対象ラボでは、所有する機器が使用目的に適合していることを実証するため、分析機器適格性評価を実施しなければなりません。アジレントは、社内の評価担当チーム(Microsoft Excel を使用)および推奨される Agilent Automated Compliance Engine(ACE)がそれぞれ実施した適格性評価を比較し、詳細に調査しました。
その結果、以下に示す ACE の利点が明らかになりました。
- 社内モデルと比較してコストを 13 % 削減
- 社内モデルと比較して機器のダウンタイムを 70 % 低減
- Excel の使用をやめることでデータインテグリティリスクを低減
- エンドツーエンドのデータトレーサビリティを確保し、21 CFR Part 11 に準拠することでワークフローを簡略化
- 社内評価チームの時間を他の重要な業務に充てることが可能に
スプレッドシートの脆弱性については以下をご覧ください。